Chapitre 1 : Chimie du corps humain
Objectifs d’apprentissage
Après avoir lu le présent chapitre, vous devriez être en mesure d’atteindre les objectifs suivants :
- Faire la différence entre un atome, un ion et une molécule.
- Faire la différence entre un élément et un composé.
- Faire la différence entre un acide, une base et un électrolyte.
- Expliquer la signification de l’échelle de pH.
- Expliquer l’importance de l’équilibre acido-basique dans le corps.
- Expliquer les termes métabolisme, anabolisme et catabolisme.
- Décrire la structure et la fonction des glucides, des protéines, des lipides et des acides nucléiques.
- Énoncer la fonction des enzymes, des substrats, des cofacteurs et des coenzymes.
- Expliquer la régulation des réactions à médiation enzymatique.
Atomes et ions
Tout comme la cellule est l’unité fondamentale de tout organisme vivant, l’atome est l’unité fondamentale de la matière.
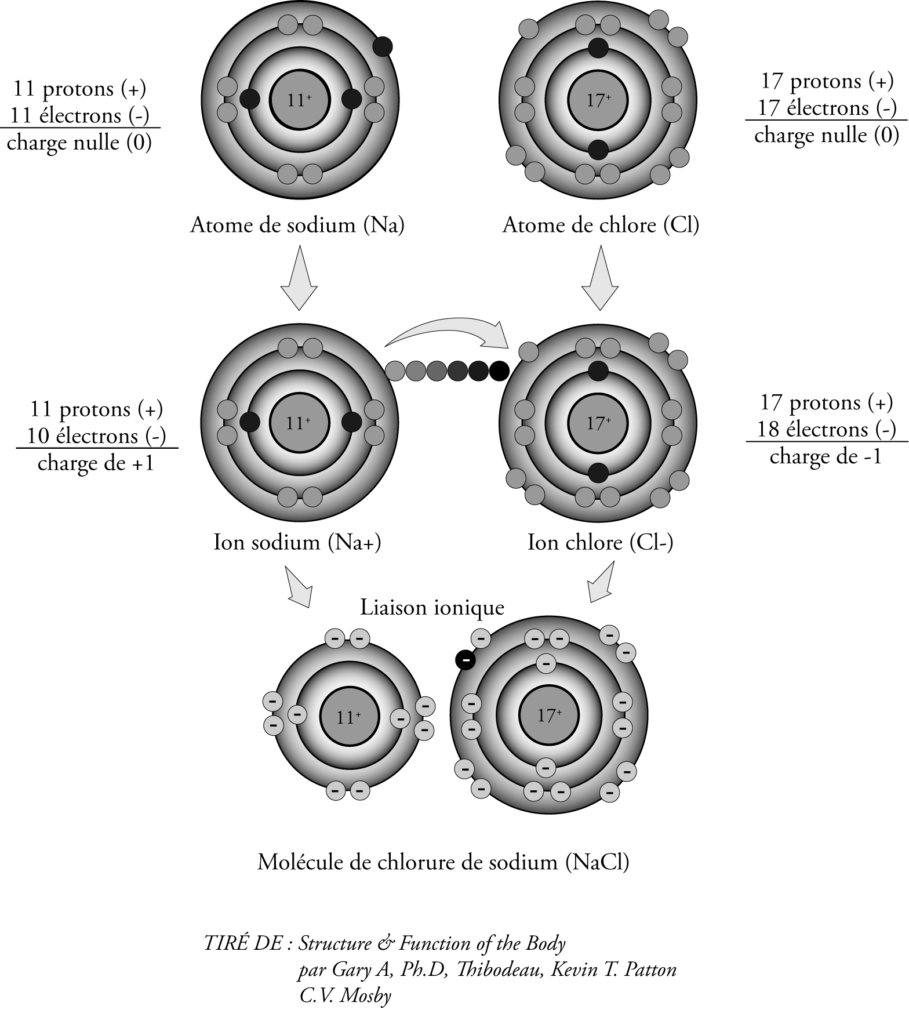
Au centre d’un atome se trouve un noyau qui contient des protons, particules de charge électrique positive, et des neutrons, particules de charge neutre. Les électrons, particules de charge électrique négative, gravitent en orbitales autour du noyau (figure 1.1-1). Puisque le nombre de protons et d’électrons est égal, l’atome n’est chargé ni positivement, ni négativement.
Les atomes possédant 8 électrons dans leur orbitale externe sont stables. Les atomes métalliques possèdent 1, 2 ou 3 électrons sur leur orbitale externe. Les atomes non métalliques possèdent 5, 6 ou 7 électrons sur leur orbitale externe. Les gaz inertes, comme le radon, ont 8 électrons et sont stables, d’où l’appellation de gaz inerte.
Pour devenir stable, l’atome métallique doit perdre les électrons qui gravitent sur son orbitale externe. L’atome non métallique peut recevoir les électrons de l’ion métallique afin de stabiliser l’orbitale externe des deux atomes métallique et non métallique.
Saviez-vous?
Les atomes sont des particules infiniment petites – des millions d’atomes pourraient tenir sur une tête d’épingle.
Si l’atome gagne un électron, il devient chargé négativement. Inversement, si l’atome perd un électron, il devient chargé positivement. Un atome chargé, soit positivement, soit négativement, porte le nom d’ion*. Les ions à charge positive se nomment cations, tandis que les ions à charge négative se nomment anions.
La figure 1.1-1 montre un atome de sodium qui entre en contact avec un atome de chlore. Ce dernier gagne un électron de l’atome de sodium, et les deux nouveaux ions (Na+ et Cl-) s’attirent mutuellement en raison de leurs charges opposées. Les ions se lient entre eux pour former le composé* chlorure de sodium. La liaison qui résulte du transfert d’électrons s’appelle liaison ionique.
Molécules
Une molécule* se forme par l’union de deux atomes ou plus. Une molécule peut contenir des atomes identiques, ou encore deux ou plusieurs atomes différents. Par exemple, une molécule d’oxygène (O2) contient deux atomes d’oxygène, alors qu’une molécule d’eau (H2O) contient deux atomes d’hydrogène et un atome d’oxygène.
Éléments et composés
Les éléments* ne contiennent qu’un seul type d’atome, et ainsi ne peuvent être décomposés en substances différentes. Il existe environ 105 éléments connus.
Les éléments qui composent la plupart des cellules du corps humain sont :
- le carbone (C);
- l’hydrogène (H);
- l’oxygène (O);
- l’azote (N).
D’autres éléments importants dans l’organisme sont :
- le fer (Fe);
- le potassium (K);
- le calcium (Ca);
- le sodium (Na);
- le phosphore (P);
- le soufre (S);
- le chlore (Cl);
- le magnésium (Mg).
Les composés sont des substances qui contiennent deux éléments ou plus. L’eau (H2O) est un exemple de composé.
Acides et bases
Un acide* est une substance chimique qui peut céder un ion hydrogène (H+) à une autre substance. L’acide chlorhydrique, acide que l’on trouve dans l’estomac, en est un exemple. L’équation ci-dessous illustre l’équilibre existant en solution entre l’acide non dissocié à gauche et ses produits de dissociation à droite.
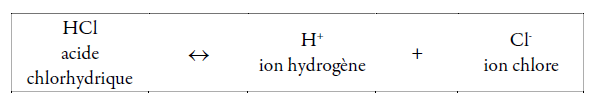
Une base* est une substance chimique qui peut accepter un ion hydrogène (H+) d’une autre substance. Les bases contiennent habituellement un ion hydroxyde (OH–). L’hydroxyde de sodium est une base. L’équation ci-dessous illustre l’équilibre existant en solution entre la base non dissociée à gauche et ses produits de dissociation à droite.

Électrolytes
Les substances qui se dissocient dans l’eau pour donner des cations (ions positifs) et des anions (ions négatifs) sont appelées électrolytes* car ces ions favorisent la conductance d’un courant électrique dans l’eau.
- Électrolytes forts — Les sels de sodium (Na) et de potassium (K) comme le chlorure de sodium (NaCl) et le chlorure de potassium (KCl) constituent de bons exemples. En solution, le NaCl se dissocie complètement pour donner des ions Na+ et Cl-, appelés des électrolytes forts.
- Électrolytes faibles — Beaucoup de médicaments sont acides ou basiques. En solution dans l’eau, ils se dissocient en ions qui agissent comme électrolytes. Cependant, bon nombre d’acides et de bases ne se dissocient pas totalement en solution. Il s’établit plutôt un équilibre entre les formes dissociées et non dissociées. Même si des anions et des cations se trouvent en solution, ils ont une capacité plus faible de transmettre un courant électrique et sont donc appelés électrolytes faibles.
- Non-électrolytes — Les sucres et les alcools ne sont pas classés parmi les électrolytes car même s’ils se dissolvent facilement dans l’eau, ils ne portent aucune charge et ne se dissocient pas en particules chargées.
L’échelle de pH
L’échelle de pH* mesure la concentration d’ions hydrogène dans une solution. La plage de valeurs s’étend de 0 à 14. Chaque unité descendante correspond à une augmentation de dix fois le nombre d’ions présents par rapport à l’unité suivante. Par exemple, une solution dont le pH est de 4,0 contient dix fois plus d’ions hydrogène qu’une solution dont le pH est de 5,0.
Plus la concentration d’ions hydrogène d’une solution est élevée, plus la solution est dite acide*. La solution la plus acide aurait un pH de 0. Plus la concentration d’une solution en ions hydrogène est faible, plus la solution est alcaline* (basique*). La solution la plus basique qui existe aurait un pH de 14.
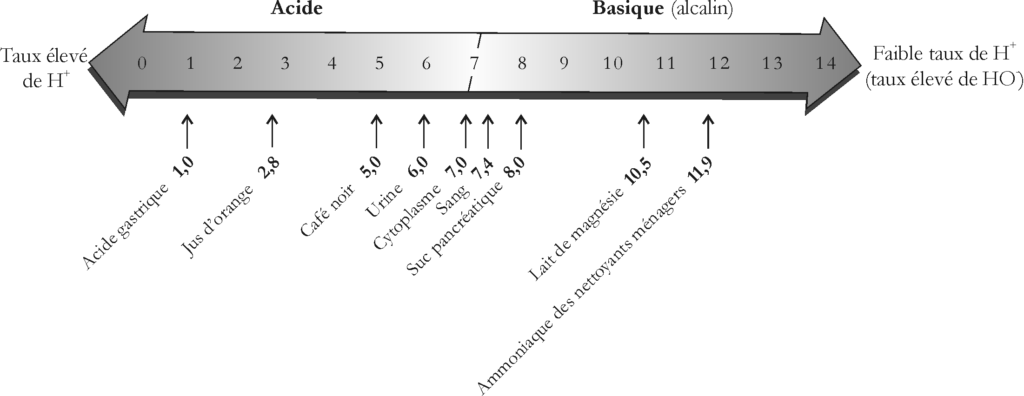
Ainsi, plus le pH est faible, plus la solution est acide, et plus le pH est élevé, plus la solution est alcaline (figure 1.1-2). Ainsi l’acide gastrique affiche un pH de 1,0 alors que le sang est légèrement alcalin, avec un pH de 7,4.
Une solution ayant un nombre égal d’ions hydrogène et hydroxyde est dite neutre et possède un pH de 7,0. L’eau pure et le cytoplasme sont des exemples de substances ayant un pH neutre.
Équilibre acido-basique dans le corps
Les acides et les bases sont des composés qui influent sur les réactions chimiques se produisant dans l’organisme. Il existe un équilibre délicat entre l’acidité et l’alcalinité des liquides organiques. Par exemple, le sang est légèrement alcalin, l’urine est légèrement acide, le suc gastrique est plus acide et les sucs intestinaux et pancréatiques sont alcalins.
L’équilibre acido-basique du corps doit être maintenu pour les raisons suivantes :
- un changement de la concentration en ions hydrogène (plus forte ou plus faible que la normale) perturbera les réactions chimiques normales du corps;
- le pH influe sur le mouvement des électrolytes à travers les membranes cellulaires et peut avoir un effet prononcé sur différentes fonctions du corps.
Si des tissus sont soumis à un degré de pH ne correspondant pas à leurs indices habituels, des lésions pourraient en résulter. Par exemple, dans le cas d’une sécrétion excessive d’acide gastrique ou d’un affaiblissement du mécanisme de défense de la muqueuse gastro-intestinale, le revêtement du tube digestif peut être exposé à l’acide gastrique et subir des lésions.
Dans le sang, le gaz carbonique (CO2) forme de l’acide carbonique (H2CO3) lorsqu’il se dissout dans l’eau. Une partie de l’acide carbonique se dissocie ensuite pour produire des ions H+ et HCO– (bicarbonate), entraînant une quantité excessive d’ions H+ dans le sang. Par conséquent, des niveaux élevés de CO2 dans le sang rendent ce dernier plus acide (acidose*). Si la teneur en gaz carbonique du sang est trop faible, le sang devient plus alcalin (alcalose*). On mesure la concentration en ions bicarbonate et le pH des échantillons sanguins pour déterminer le bilan acido-basique d’un patient. Dans des conditions normales, les poumons et les reins travaillent ensemble pour réguler l’équilibre acido-basique du sang, maintenant le pH et la teneur en CO2 dans des plages strictes. Les poumons accomplissent leur fonction en régissant la quantité de CO2 dans le sang (c.-à-d., les poumons éliminent le CO2 dans l’air expiré). Il revient aux reins de réguler la teneur en HCO3–, composante basique du pH (c.-à-d., les reins réabsorbent tout le bicarbonate qui est éliminé du sang par filtration). Le rôle des poumons dans le maintien de l’équilibre acido-basique sera abordé en détail dans le Module 5, chapitre 2, et celui des reins, dans le Module 7, chapitre 2.
Métabolisme
Beaucoup de réactions chimiques et physiques surviennent dans les cellules du corps pour le maintenir en vie. Ces réactions cellulaires constituent le métabolisme*.
Le métabolisme comporte deux types de réactions :
- le catabolisme*;
- l’anabolisme*.
1) Catabolisme
Le catabolisme est un processus métabolique de destruction au cours duquel les substances complexes sont décomposées en substances plus simples, avec libération d’énergie. Par exemple, le catabolisme est responsable de la dégradation des nutriments stockés, comme le glycogène* et la graisse, en unités plus simples que les cellules du corps peuvent utiliser sous forme d’énergie.
2) Anabolisme
Au cours de l’anabolisme, les composés simples sont convertis en substances complexes nécessaires à certaines activités cellulaires comme la croissance, le fonctionnement et la réparation des cellules. Ce processus permet aussi de constituer des réserves d’énergie. La conversion du glucose en glycogène représente un exemple d’anabolisme.
Composés organiques
Les composés organiques* contiennent tous un élément de carbone.
Le carbone a la capacité de s’unir à différents éléments, et plusieurs atomes de carbone peuvent s’unir pour former de longues chaînes. Ainsi, la plupart des composés organiques sont de grosses molécules complexes.
Il existe quatre types de composés organiques :
- les glucides*;
- les protéines*;
- les lipides*;
- les acides nucléiques*.
Nous étudierons chacun de ces composés organiques en détail. Chaque composé est constitué d’éléments qui, comme des pièces d’assemblage, concourent à former le composé.
1) Glucides
Les glucides contiennent du carbone, de l’hydrogène et de l’oxygène.
Les monosaccharides*, qui sont des sucres simples, sont les éléments constitutifs des glucides. L’union de monosaccharides forme des polysaccharides*, qui sont des glucides complexes.
Les glucides constituent la principale source d’énergie du corps. Le glucose, sucre simple présent dans le sang, est une source d’énergie facilement utilisable pour les cellules. Le glucose est stocké sous forme d’amidon dans les plantes et de glycogène chez les animaux. L’amidon et le glycogène sont des polysaccharides composés d’un grand nombre d’unités de glucose.
2) Protéines
Les protéines contiennent de l’azote en plus du carbone, de l’hydrogène et de l’oxygène. Certaines protéines peuvent également contenir du soufre, du phosphore et du fer. Les protéines sont formées à partir d’acides aminés*, rassemblés pour constituer une longue chaîne. Le nombre d’acides aminés, leur type et leur séquence dans la chaîne déterminent la structure primaire d’une protéine. La longue chaîne peut se replier sur elle-même pour former une protéine globulaire. Chaque protéine possède une configuration spatiale spécifique, caractéristique qui a permis la mise au point de traitements ciblés.
Les protéines sont le principal matériau de construction du corps humain. On les trouve dans les os, les muscles et le tissu conjonctif. Elles sont essentielles à la formation, à la croissance et à la réparation des tissus. Les pigments des cheveux, des yeux et de la peau contiennent également des protéines.
3) Lipides
Les lipides sont un autre type de composé organique, les plus connus étant les graisses et les substances apparentées qui permettent de conserver l’énergie à long terme. Ils isolent et protègent également les organes. Les éléments constitutifs des graisses sont le glycérol* et les acides gras*.
Il existe plusieurs types importants de lipides dans l’organisme :
- les triglycérides* — Les triglycérides sont des molécules lipidiques formées par une unité de glycérol liée à trois acides gras. La rupture de ces liaisons libère de l’énergie. Les triglycérides servent à stocker l’énergie dans les cellules pour un usage ultérieur.
- les phospholipides* — Les phospholipides ont sensiblement la même structure que les triglycérides, sauf qu’un acide gras est remplacé par un groupe phosphate (PO4). Les phospholipides comprennent une tête hydrophile* (groupe phosphate) et une queue hydrophobe* (deux acides gras). Cette structure leur permet de former une bicouche* stable dans l’eau qui constitue la base des membranes
- les stéroïdes* — Le cholestérol* est un important stéroïde. Il se lie avec les phospholipides de la membrane cellulaire pour en stabiliser la structure en bicouche. Le cholestérol est utilisé dans la synthèse des hormones* stéroïdiennes comme les œstrogènes*, la testostérone* et la cortisone*.
4) Acides nucléiques
Deux formes d’acides nucléiques se trouvent dans les cellules : l’acide désoxyribonucléique (ADN)* et l’acide ribonucléique (ARN)*
- Acide désoxyribonucléique (ADN)
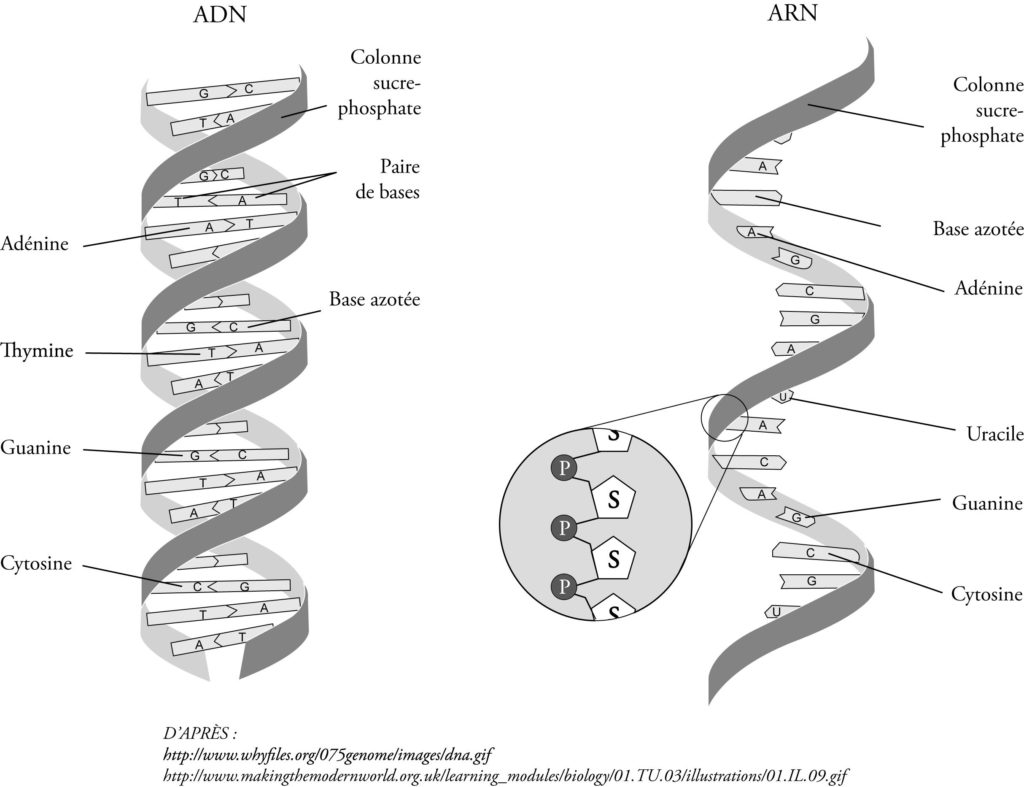
Les molécules d’acide désoxyribonucléique (ADN) sont des macromolécules composées de deux brins liés entre eux pour former une double hélice (figures 1.1-3 et 1.1-4).
Chaque brin se compose d’unités répétées, appelées nucléotides*. Chaque nucléotide contient un groupe phosphate, le sucre appelé désoxyribose et une base azotée. Il existe quatre types de bases : l’adénine (A), la guanine (G), la cytosine (C) et la thymine (T). En raison de leur composition chimique, l’adénine se lie à la thymine, et la guanine se lie à la cytosine. Ces liaisons unissent les deux brins d’ADN.
Le nombre, le type et la disposition des bases d’ADN déterminent la sorte de protéine que la cellule peut former. Le chapitre 2 traitera en détail de l’importance de l’ADN dans la détermination de la constitution génétique des cellules.
- Acide ribonucléique (ARN)
L’acide ribonucléique (ARN) a une structure similaire à celle de l’ADN, mais il est composé d’un seul brin (figure 1.4-3).
L’ARN contient la base uracile (U) au lieu de la thymine, et le sucre ribose au lieu du désoxyribose. L’uracile a la capacité de se lier à l’adénine.
L’ARN est aussi nécessaire pour la formation de protéines dans la cellule. Le chapitre 2 traitera du rôle de l’ARN dans la synthèse des protéines.
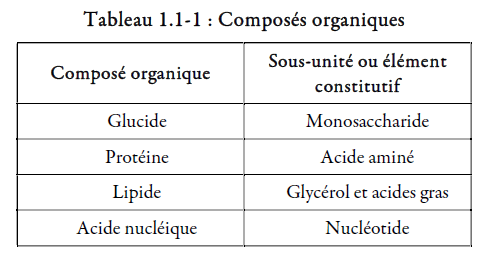
Figure 1.1-3 : Nucléotides de l’ADN (schéma de ses 4 bases azotées)
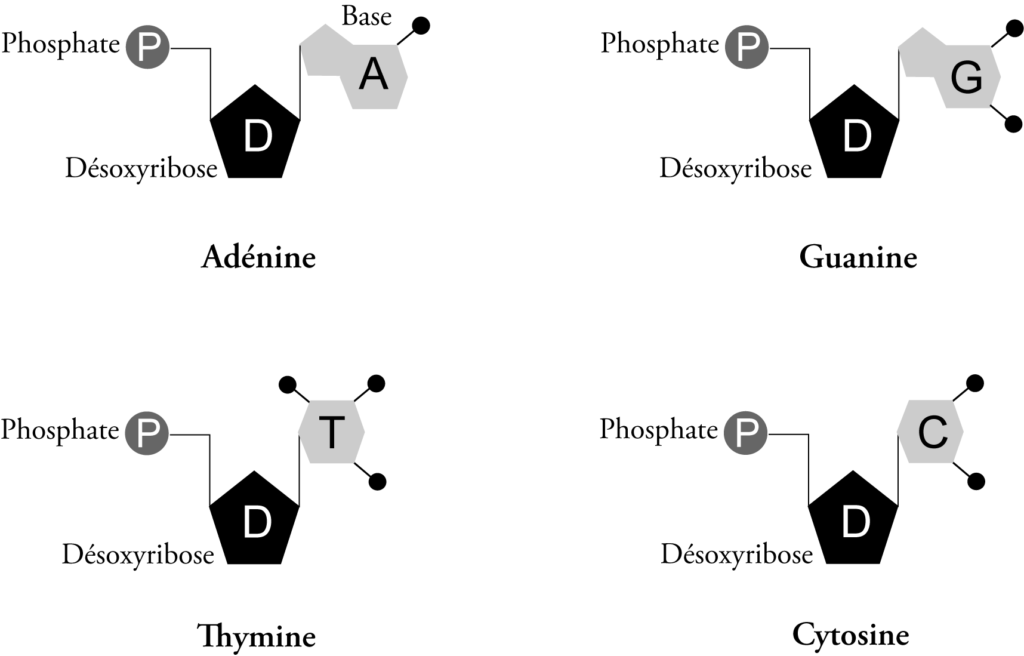
Figure 1.1-4 : Structure de l’ADN et de l’ARN
Enzymes
Les enzymes* constituent un groupe important de protéines. Il s’agit de catalyseurs organiques qui accélèrent la réaction métabolique, sans être modifiés ni consumés pendant le processus. Chaque réaction chimique ayant lieu dans l’organisme exige la participation d’une enzyme spécifique.
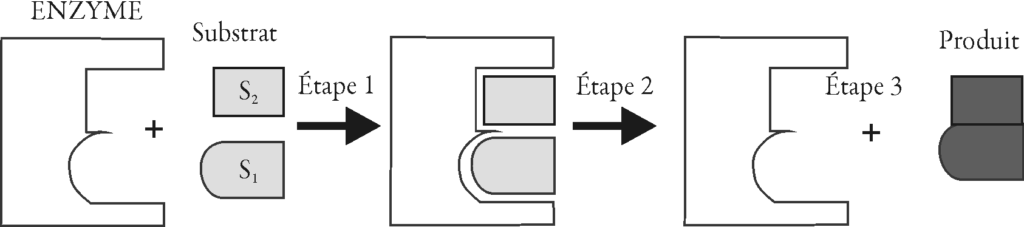
La conversion d’un substrat* en un nouveau produit exige la présence d’une enzyme. En présence de l’enzyme appropriée, les substrats sont capables de se lier aux sites actifs de l’enzyme, de réagir et de former un nouveau produit (figure 1.1-5).
Parfois, une enzyme nécessite la présence d’une autre substance appelée cofacteur afin d’accomplir sa tâche correctement. Les oligoéléments comme le fer, le magnésium et le calcium sont des exemples de cofacteurs. On appelle coenzyme un cofacteur qui est une substance organique.
Figure 1.1-5 : Action enzymatique
Facteurs qui influent sur les réactions à médiation enzymatique
La vitesse d’une réaction à médiation enzymatique peut être modifiée par l’un des facteurs suivants :
- la concentration de substrats;
- la concentration d’enzymes;
- l’activité enzymatique.
1) Concentration de substrats
Un changement de la quantité des substrats dans une cellule a des répercussions sur la vitesse de la réaction métabolique. Une augmentation de la quantité de substrats entraîne une augmentation de la vitesse tant que les sites actifs des enzymes ne sont pas saturés par le substrat. Une fois la vitesse maximale atteinte, la vitesse de réaction demeure constante indépendamment de la quantité de substrats présente.
2) Concentration d’enzymes
Une augmentation de la quantité d’enzymes disponibles se traduit par une augmentation de la vitesse de réaction à médiation enzymatique, car le substrat dispose d’un plus grand nombre de sites actifs pour se fixer.
3) Activité enzymatique
Plusieurs facteurs peuvent influer sur l’activité d’une enzyme. Ainsi, on peut empêcher une enzyme de jouer son rôle de catalyseur dans une réaction métabolique normale en ajoutant un substrat de compétition, qui se lie à l’enzyme à la place du substrat normal. Si une substance dont la forme ressemble à un substrat normal est présente, elle peut occuper le site actif sur l’enzyme et en inhiber l’activité sur le substrat normal.
Les températures ou les variations d’acidité extrêmes peuvent aussi modifier la forme d’une enzyme, ce qui a pour effet d’en diminuer l’activité.
Résumé — Chapitre 1 : Chimie du corps humain
Toute matière, qu’elle soit organique ou non, est formée d’éléments chimiques et de composés :
- l’atome – unité fondamentale de la matière contenant des protons, des électrons et des neutrons;
- la molécule – union de deux atomes ou plus, lesquels peuvent être identiques ou non;
- l’élément – union de plusieurs atomes du même type;
- le composé – union d’au moins deux éléments différents.
Une liaison ionique se forme lorsque des atomes ou des groupes d’atomes sont attirés les uns vers les autres et se lient par un échange d’électrons. Comme ces derniers sont chargés négativement, l’ajout d’électrons donne une charge négative alors que la perte d’électrons donne une charge positive. Dans un composé ionique, les ions demeurent liés entre eux grâce à l’attraction entre charges opposées. Lorsqu’ils sont chauffés ou dissous en solution, les composés ioniques se dissolvent et assurent la conductance de l’électricité; leurs particules individuelles sont appelées des électrolytes. Les composés qui ne se dissocient pas entièrement en solution (dont les sels et les acides) ont une faible capacité de porter une charge électrique, d’où l’appellation d’électrolytes faibles.
Les acides et les bases sont des composés qui participent aux réactions chimiques se produisant dans l’organisme. Le degré d’acidité est mesuré par le pH. Le pH de divers liquides organiques peut varier entre un haut niveau d’acidité dans l’estomac et un faible niveau d’acidité (c.-à-d., un niveau d’alcalinité plus élevé) dans les intestins. L’équilibre acido-basique sanguin est maintenu dans un écart étroit par les actions jumelées des poumons et des reins, qui compensent les modifications du taux de gaz carbonique (CO2) ou de pH.
Le métabolisme fait référence aux réactions chimiques et physiques qui surviennent dans le corps afin de le maintenir en vie. L’anabolisme assure la formation (synthèse) cellulaire des molécules organiques ou le stockage de l’énergie. Le catabolisme est la destruction cellulaire des molécules organiques ou la libération d’énergie en vue de la consommation par les cellules.
Le corps est constitué de quatre principaux composés organiques, dont voici la liste ainsi que leurs sous-unités :
- les glucides – monosaccharides (sucres simples) et polysaccharides;
- les protéines – acides aminés;
- les lipides – glycérol et acides gras;
- les acides nucléiques (ADN et ARN) – nucléotides.
Les enzymes sont des protéines qui modifient la vitesse à laquelle surviennent les réactions métaboliques. Parmi les facteurs qui influent sur les réactions à médiation enzymatique, soulignons :
- la concentration de substrats;
- la concentration d’enzymes;
- l’activité enzymatique.
Autoévaluation — Chapitre 1 : Chimie du corps humain
1 Appariez la description de la colonne A et le terme correspondant de la colonne B.
| Colonne A | Colonne B | |
| 1) atome de charge positive | _____ | a. proton |
| 2) particule de charge négative qui entoure le noyau de l’atome | _____ | b. neutron |
| 3) substance contenant un seul type d’atome | _____ | c. électron |
| 4) particule de charge positive dans le noyau de l’atome | _____ | d. ion |
| 5) ions qui assurent la conductance de l’électricité lorsque mis en solution | _____ | e. cation |
| 6) substance dont le pH est de 3,0 | _____ | f. anion |
| g. élément | ||
| h. molécule | ||
| i. composé | ||
| j. électrolyte | ||
| k. acide | ||
| l. base |
2 Plus la concentration d’ions hydrogène dans une solution est élevée, plus la solution est acide
a) Vrai
b) Faux
3 Pourquoi l’équilibre acido-basique des liquides organiques est-il essentiel au maintien de la santé?
_____________________________________
_____________________________________
_____________________________________
_____________________________________
4 Définissez les termes suivants :
1 Métabolisme
_________________________________
_________________________________
_________________________________
2 Catabolisme
_________________________________
_________________________________
_________________________________
3 Anabolisme
_________________________________
_________________________________
_________________________________
5 Pour chacun des principaux composés organiques, énoncez l’élément constitutif ou la sous-unité.
glucides ___________________________
protéines __________________________
lipides ____________________________
acides nucléiques _____________________
6 Le cholestérol est une composante importante des __________ et des __________.
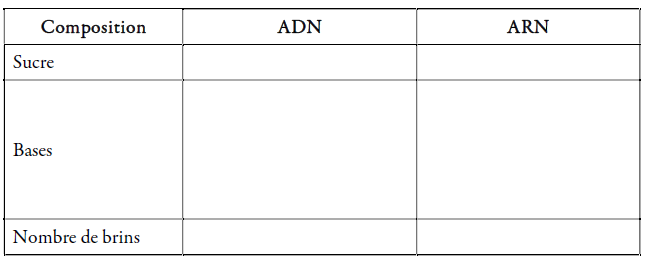
7 Comparez la structure de l’ADN à celle de l’ARN en remplissant le tableau suivant.
8 Énoncez la fonction des enzymes dans une cellule.
____________________________________
____________________________________
9 Énumérez trois facteurs qui influent sur les réactions à médiation enzymatique dans les cellules.
1 ________________________________
2 ________________________________
3 ________________________________
10 Indiquez 3 facteurs qui pourraient perturber l’activité enzymatique.
1 ________________________________
2 ________________________________
3 ________________________________
Corrigé de l’Autoévaluation — Chapitre 1 : Chimie du corps humain
1
1) e. cation
2) c. électron
3) g. élément
4) a. proton
5) j. électrolyte
6) k. acide
2
a) Vrai
3
Si le pH des liquides organiques est modifié, les réactions chimiques normales et les fonctions du corps sont perturbées, ce qui peut entraîner des lésions dans les tissus.
4
1 Métabolisme – Réactions physiques et chimiques qui s’opèrent dans les cellules pour maintenir l’organisme en vie
2 Catabolisme – Dégradation de substances complexes en substances plus simples avec libération d’énergie en vue de la consommation par les cellules
3 Anabolisme – Constitution de substances plus complexes et stockage d’énergie
5
glucides _ monosaccharides
protéines _ acides aminés
lipides _ glycérol et acides gras
acides nucléiques _ nucléotides
6
hormones stéroïdiennes (p. ex., œstrogènes, testostérone, cortisone)
membranes cellulaires
7
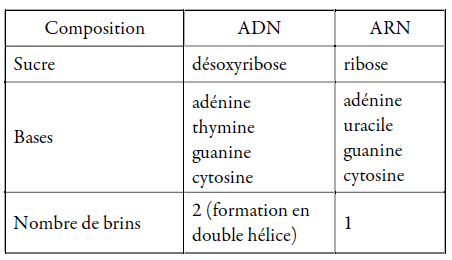
8
Les enzymes sont des catalyseurs organiques qui accélèrent la réaction dans les cellules, mais qui ne subissent aucun changement ou qui ne sont pas consumés pendant le processus.
9
1 concentration de substrats
2 concentration d’enzymes
3 activité enzymatique
10
1 emploi d’un substrat de compétition
2 températures extrêmes
3 variations de l’acidité de la cellule
